
PHERAstar FSX
功能强大,高度灵敏的HTS酶标仪


该技术基于高灵敏度检测能力,可稳定采集闪光型与辉光型生物发光信号,适用于报告基因分析、ATP 定量检测等多种应用场景。
“发光(Luminescence)”一词来源于拉丁语“lumin”(光)与后缀“-escence”(表示过程或状态变化),本质上指的是一种非热辐射的光释放过程。发光的核心特征在于其“冷光”属性,即光的产生不依赖高温热辐射,因此与炽热物体通过高温产生的白炽发光(incandescence,如燃烧的蜡烛或炽热金属)具有明确区别¹。
发光信号可由多种能量形式转化而来,其本质是将不可见能量(如化学能或光能)转化为可见光辐射。在自然界中,发光可作为生物防御或信号传递机制(如生物发光现象);在技术领域,则广泛应用于显示技术(如LED)及分析检测体系。本文重点讨论发光技术在生命科学中的应用,并围绕其物理原理、发光酶标仪的检测机制及常见微孔板发光实验进行说明。电致发光、放射发光及热致发光由于不属于本文讨论范围,在此不作展开。
发光是能量转化产生发光信号的过程。在生命科学领域,发光主要依赖两类能量输入方式:化学能与光能,分别对应化学发光(chemiluminescence)与光致发光(photoluminescence)。其中,光致发光亦构成荧光及磷光现象的基础物理过程。
当分子吸收外界能量后,其电子从基态跃迁至激发态(见图1)。由于激发态在能量上不稳定,电子会在返回基态过程中发生能量弛豫,部分能量以非辐射形式(振动能、热能)释放,另一部分则以光子形式释放,从而产生发光信号²。
在生命科学领域,磷光与光致发光通常被统称或简化为“荧光”;而“发光”一词在实际应用语境中往往特指化学发光。这种术语简化也体现在检测方式的本质差异上:荧光检测依赖外部激发光源,而发光检测无需激发光源(图2)。本文遵循该领域的常用表达习惯,重点讨论化学发光,并在后续内容中统一以“发光”指代化学发光体系。
在化学发光反应中,底物在反应过程中转化为电子激发态的中间体或产物。当这些处于激发态的分子回到基态时,其电子发生能级跃迁并以光子的形式释放能量,从而产生发光信号。典型例子为鲁米诺(luminol)在过氧化氢存在下的反应(图3):在碱性条件下,鲁米诺以二价阴离子形式与分子氧(O₂)发生氧化反应,生成处于电子激发态的3-氨基邻苯二甲酸(3-APA)。随后,该产物从激发态回到基态过程中释放光子,产生可检测的发光信号。
这一基本反应机制构成了多种增强型化学发光体系及生物发光体系的理论基础。从能量转化本质来看,两者均属于化学发光反应在不同体系中的延伸应用。
增强化学发光是指在化学发光反应中加入增强剂,从而提高发光信号强度与稳定性的一类检测技术。该体系通常以鲁米诺(luminol)与过氧化氢为基础反应体系,并在辣根过氧化物酶(HRP)的催化作用下发生氧化反应。由于酶能够催化特异性生化反应,增强化学发光常用于各类酶联检测体系。其中最典型的应用是免疫印迹(immunoblotting):首先通过凝胶电泳按分子量分离蛋白质,并将其转移至膜上;随后通过特异性一抗识别目标蛋白,再加入HRP标记的二抗,使酶与抗原–抗体复合物结合。加入底物及增强体系后,仅在目标蛋白所在区域发生显著发光反应,从而形成清晰的检测信号。
在基于微孔板的生物分子定量分析中,该原理同样适用。例如在发光型酶联免疫吸附实验(ELISA) 中,目标蛋白固定于微孔板孔底,通过抗体体系与HRP标记二抗形成复合物,在底物与增强剂共同作用下产生发光信号,其强度与目标蛋白浓度呈正相关,从而实现高灵敏度定量检测。
生物发光存在于生命体中,是指生物体通过自身代谢反应产生可见光的现象。该术语在实验与应用语境中通常涵盖两类体系:一类是直接使用来源于天然生物的酶与底物,即使在体外体系中仍可保持其发光反应;另一类则通过基因工程手段对相关发光蛋白或底物体系进行优化或重构,以获得更适用于实验检测的性能。
在自然界中,生物发光具有多种生理功能。例如,萤火虫通过发光进行配偶吸引;维多利亚水母(Aequorea victoria)以及部分深海磷虾等生物,被认为可利用发光进行防御或干扰捕食者;海洋细菌费氏弧菌(Vibrio fischeri)则可在群体密度达到阈值后,通过群体感应(quorum sensing)调控发光行为,从而实现种群间的信息交流与行为协同。
从分子机制来看,生物发光的核心过程是由荧光素酶(luciferase)催化荧光素(luciferin)发生氧化反应,在此过程中生成电子激发态产物,并在其回到基态时释放光子。不同生物体系使用的荧光素酶与荧光素类型各不相同,同时反应所需辅因子及发光波长也存在差异。图4展示了生命科学实验中常用的三种典型荧光素酶发光反应体系。 
共振能量转移(Resonance Energy Transfer)指电子激发态的供体分子向受体荧光团转移能量的过程。受体在获得能量后被激发,并进一步以光子形式释放荧光信号。当该过程中的供体能量来源于生物发光反应时,则称为生物发光共振能量转移(bioluminescence resonance energy transfer, BRET)。
BRET 的发生需要满足若干关键条件:其一,供体的发射光谱需与受体荧光团的激发光谱具有足够重叠,以保证能量转移的谱学基础;其二,供体与受体必须在空间上保持足够接近,通常距离为 1–10 nm,因为能量转移效率随距离增加呈快速衰减。因此,BRET 常被用于检测生物分子之间的相互作用或空间接近关系。
BRET 的检测输出通常以比值形式表示,即受体发光强度与供体发光强度之比(BRET ratio)。不同体系如 BRET1、BRET2 及 NanoBRET 采用不同的荧光素酶与受体荧光团组合,以适配不同的检测需求(见表1)。
表 1:BRET 类型表
|
名称 |
供体荧光素酶 |
底物 |
供体发射波长 |
受体荧光团 |
受体发射波长 |
|
BRET 1 |
Renilla |
Coelenterazine |
450-500 nm |
YFP |
515-560 nm |
|
GFP |
510-540 nm |
||||
|
BRET 2 |
Renilla |
DeepBlueC |
400-450 nm |
GFP |
500-540 nm |
|
NanoBRET |
NanoLuc |
Furimazine |
420-500 nm |
NanoBRET 618 |
550-675 nm |
|
TMR |
550-600 nm |
||||
|
AlexaFluor 633 |
600-700 nm |
||||
|
Venus |
515-575 nm |
生命科学领域的发光检测分为闪光型(flash)和辉光型(glow)两种反应类型,其主要区别在于信号持续时间与反应动力学特征。闪光型发光信号通常在反应启动后的数秒内迅速达到峰值并快速衰减,因此需要对整个发光过程进行连续记录。闪光型反应通常通过加入启动试剂瞬时触发,实验过程对时间同步性要求较高,因而发光检测系统通常需要配备自动注射装置,以实现试剂加入与信号采集的精确同步。常见的闪光型发光应用包括双荧光素酶报告基因检测(Dual-Luciferase Reporter™ technology )以及SPARCL(SPARCL assays) 等。
与闪光型发光相比,辉光型发光具有更为稳定的信号输出特征,其发光信号可在较长时间内保持相对恒定,持续时间可达数小时甚至更久。因此,该类反应通常无需严格的同步加样或实时启动控制,可在较为灵活的时间窗口内完成检测。
由于操作流程简化、稳定性更高,辉光型发光体系在实验应用中更为常见。细胞活性检测实验CellTiter-Glo®是辉光型发光技术最具代表性的应用之一。
除免疫印迹中的增强化学发光检测外,发光实验通常采用微孔板(6 孔至 1536 孔)作为反应与检测载体 ,并通过酶标仪进行定量检测。本节将重点介绍微孔板中发光的检测原理与过程。
相较于荧光或吸光度检测,发光检测体系结构更为简化,其关键优势在于无需外部激发光源,因此也无需激发光波长选择与滤光系统。发光检测的基础光学组成主要包括两部分:用于收集发光信号的光学透镜系统,以及用于信号转换与记录的光电检测器(图5)。若需检测生物发光共振能量转移(BRET),则需配备波长分离或光谱筛选组件;在部分特定光路设计中,为提升信号传输效率或适配复杂检测模式,也可引入光导纤维作为辅助传光结构。 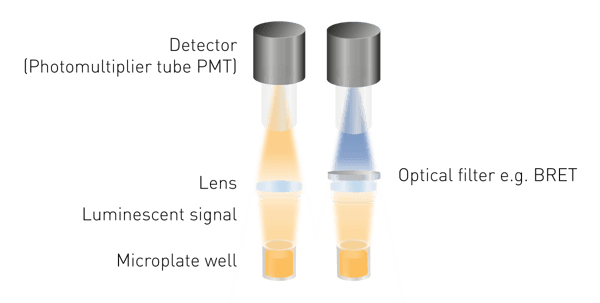
光电倍增管(photomultiplier tube, PMT) 是发光检测中的核心检测器。不同光电倍增管在灵敏度(最低可检测信号水平)、噪声水平以及对多种检测模式的兼容性方面存在差异。 许多检测设备配备通用型光电倍增管,可同时用于发光、吸光度及荧光等检测模式。这类PMT的优势在于结构紧凑、成本相对较低,同时仍可提供较高的检测灵敏度。通过优化光学路径设计,可进一步提升弱信号检测能力。例如,PHERAstar FSX 酶标仪中采用的 “自由空气光路(free-air optical path)” 与 “增强型发光光学模块(luminescence plus optic module)” 组合,即通过光学系统优化提高了发光信号的收集效率与检测性能。
专用于发光检测的专用型PMT通常通过降低本底噪声或采用光子计数(photon counting)模式来提升检测灵敏度。尽管这类系统在低信号检测中表现优异,但光子计数架构在高信号条件下可能出现动态范围受限的问题(图6)。 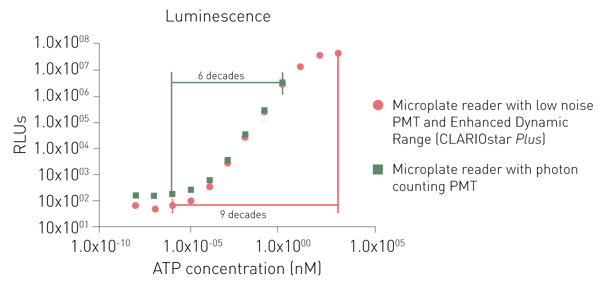
理想情况下,检测器应直接位于微孔板孔的正上方,以最大限度提高光信号收集效率。当受限于光路布局无法实现该结构时,可通过光导纤维(或结合透镜与反射镜系统)将微孔中产生的发光信号导向检测器。光导纤维会吸收部分发光信号,相较于“自由空气光路”结构,其整体检测灵敏度会有所降低。VANTAstar、CLARIOstar Plus 和 PHERAstar FSX 酶标仪均采用自由空气光路设计,以提升信号收集效率与检测性能。
在部分应用中,需要对特定波长范围内的发光信号进行选择性检测。这一功能通常通过在光路中引入光学滤光片或光栅分光元件实现。对于生物发光共振能量转移(BRET)检测而言,波长筛选是必要步骤,因为同一样品中同时存在供体与受体两类发光信号,必须通过不同滤光条件对其进行区分与定量。
在筛选型发光检测和生物发光共振能量转移检测中,传统的光栅(grating-based monochromators)的分光方式由于存在光散射损失及带宽较窄等因素,灵敏度相对受限,因此应用范围有限。相比之下,线性可变滤光片(linear variable filter, LVF)技术结合了滤光片式的高透光效率与连续波长选择能力,其带宽可达约100 nm,可在保证信号强度的同时实现有效波长分离,因此更适用于BRET等对灵敏度要求较高的筛选型发光检测体系(图7)。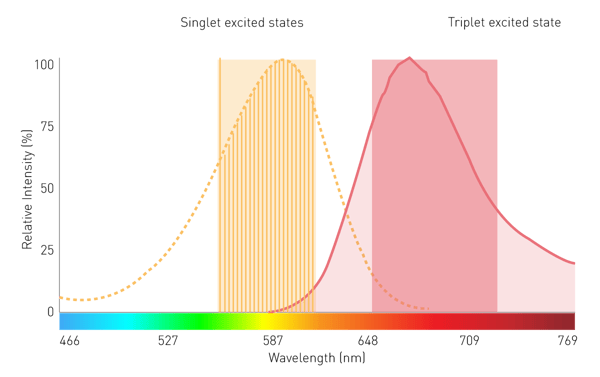
发光信号的持续时间通常在秒级或更长,而荧光信号则多在纳秒至微秒尺度内衰减,二者在时间特性上存在明显差异。因此,发光检测进行时间段检测信号采集方式,常见时间范围约为0.1–1秒。
这一参数在不同系统中可有多种表述方式,包括检测时间 (measurement time/measurement interval time )或积分时间(integration time)。其具体设置需综合考虑信号强度、动态范围以及整块微孔板的总检测时间,从而在灵敏度与检测效率之间取得合理平衡。
酶标仪发光检测整体操作较为简便,通常所需参数设置较少,但仍存在一些与仪器性能及实验设计相关的关键变量,会显著影响数据质量与可重复性。
如前所述,积分时间(采集时间)的设定需综合多方面因素进行优化,重点包括以下几个方面:
在多数实验体系中,发光信号强度足以在较短时间内完成有效采集,通常仅需0.02–0.5秒即可获得稳定读数。在少数需要区分细微信号差异的应用中,可适当延长积分时间至数秒,以提高信噪比与分辨能力。
辉光型发光信号较为稳定,因此积分时间通常设置在0.1–1秒范围内,对总体检测结果影响较小。相较之下,闪光型发光信号持续时间极短(通常仅数秒),因此必须覆盖完整的信号发生过程。
若需解析闪光型反应的动力学曲线或最大发光强度,应采用短积分时间进行连续采样。例如,对于约1秒持续的反应,可设置50次、每次0.02秒的连续检测,从而完整重建信号随时间的变化与衰减过程。
该参数主要用于动力学或时间依赖性实验。在细胞或生化反应监测中,信号变化的时间尺度直接决定积分时间与采样频率的设定。例如在钙信号检测中,刺激后约20秒内出现瞬态响应,可采用“每2秒采集一次,共10次”的方式记录全过程。
当仅检测单孔时,可适当延长积分时间(如1–2秒)以获得更高信号质量;但在多孔同步检测条件下,为维持统一时间分辨率(如每2秒记录一次所有孔数据),则需缩短单孔积分时间,以避免扫描周期过长导致时间信息丢失。
由于每个孔均需独立积分,积分时间会直接累积影响整块微孔板的总检测时间。例如,每孔仅增加0.2秒,在96孔板中将额外增加约20秒,在384孔板中则可能增加1分钟以上。因此,在高密度微孔板(384或1536孔)及高通量筛选应用中,应优先选择较短积分时间,以提升整体检测效率。
增益可视为一种放大系数,能使固定的动态范围窗口沿样品浓度曲线移动。低信号样品通常需要较高增益,而高信号样品则需降低增益以避免饱和。 通常,增益会调整至 “使预期信号最强的样品达到最大检测输出” 的水平,从而获得尽可能宽的动态信号范围。因此,当实验中包含阳性对照时,可基于其信号强度进行增益优化设定。 通过设置不同增益,检测系统可以在不同信号强度条件下实现动态范围的检测。
其中,并非所有发光酶标仪都需要手动设置增益,其是否可调以及调节方式,主要取决于检测器类型及增益控制的自动化程度。
在现代发光检测系统中,增益调节越来越多地实现自动化,不仅降低了实验操作复杂度,也提高了不同实验之间数据的一致性,并确保在单次检测中覆盖更宽的信号动态范围。例如,CLARIOstar® Plus 和 VANTAstar® 仪器搭载的 “动态范围扩展(Enhanced Dynamic Range)技术”,即可实现自动增益优化与动态范围自适应调整。
在发光检测中,白色微孔板通常是最优选择,因为其内表面具有较高反射率,能够有效反射孔内产生的发光信号,从而提高信号收集效率与检测灵敏度。关于微孔板选择的进一步细节,可参考 《微孔板:实际应用价值》("The microplate: utility in practice")。
需特别注意:当同一微孔内需同时进行发光与荧光检测时,应优先选择黑色微孔板。在白色微孔板中进行荧光检测时,由于激发光在孔壁多次反射,会显著增加背景信号并降低信噪比,导致检测结果不稳定。相比之下,在黑色微孔板中进行发光检测虽然会在一定程度上降低信号强度(检测窗口收窄),但同时也能显著降低背景干扰,从而提高测量的准确性与一致性,在实际应用中仍可获得可靠的检测结果。
信号串扰(Cross-Talk)指检测器非特异性地检测到 “非目标检测孔” 的发光信号,进而干扰 “实际检测孔” 信号的现象。该问题主要存在于发光检测中,是由发光信号的空间扩散特性所引起的典型误差来源。
由于发光反应产生的光具有扩散性,,不仅可沿垂直方向向上发射,还可能通过空气散射或孔板结构向相邻孔传播,并在后续检测过程中被检测器误读为目标信号。这种干扰会导致背景升高、数据变异增大,并降低整体检测灵敏度与准确性。根据反应类型和信号扩散特性,可采用不同策略降低或避免串扰:
对于仅持续几秒的闪光型实验,可通过优化读板顺序来减少串扰影响。由于闪光信号衰减迅速,仅当相邻孔连续检测时,才会受到串扰影响;若检测顺序改为“先检测距离较远的孔,再检测相邻孔”,则因信号已衰减至无法检测的水平,串扰会大幅降低。BMG LABTECH 酶标仪提供“交错读数模式(interlaced reading mode)”,通过先检测间隔孔位,再返回检测剩余孔位,使相邻孔之间的时间间隔延长,从而有效降低串扰影响。
辉光型实验的信号稳定且持续数小时,需采用其他策略消除串扰。干扰信号主要通过两种路径到达检测位点:其一为通过孔板上方空间的光扩散,其二为通过微孔壁或板材结构的侧向光传导(图8)。针对这两种路径,需采取不同的解决方法:
“遮光孔罩(Apertures)” 可从物理方式阻挡 “从微孔上方扩散至检测器” 的干扰信号。遮光孔罩是一种黑色勺状配件,中部设有通光孔,使用时需置于微孔板上方(图 8)。在检测过程中,目标孔的发光信号可通过中央开口进入光学系统并被检测器采集,而来自周围孔位的散射光则被遮光结构有效阻挡。
BMG LABTECH 的多功能酶标仪(PHERAstar FSX、VANTAstar 和 CLARIOstar Plus)均配备了用于提升发光检测性能的遮光孔罩。

即使是白色微孔板,发光信号仍可能通过微孔壁发生侧向扩散,形成“穿壁串扰”。该现象与微孔板结构密切相关,不同板型对串扰程度影响显著。一般而言,高密度微孔板(如1536孔板)由于孔间壁更薄,光学泄漏更为明显,因此穿壁串扰通常高于低密度微孔板。微孔形状同样会影响串扰水平:方形孔由于相邻孔共享孔壁,光传播路径更直接,串扰相对更高;圆形孔则不与相邻孔共用直壁结构,因此串扰相对较低。此外,微孔板颜色也会影响光泄漏程度,颜色越深,穿壁串扰越低;灰色微孔板在降低串扰与保持一定反射信号之间提供了折中方案。
若无法通过优化微孔板类型减少串扰,可对采集到的数据进行数学校正。其基本思路是先确定信号在相邻孔之间的泄漏比例,再基于该传递关系对原始数据进行算法校正,从而恢复真实信号分布。
BMG LABTECH 的 PHERAstar FSX、VANTAstar 和 CLARIOstar Plus酶标仪均具备自动检测并校正串扰的功能,以提高高密度板检测的准确性。
白色微孔板具有固有磷光特性,在受到光照后可能产生短暂的自发发光现象。这种自发发光信号会干扰检测数据,导致空白信号升高、压缩信号动态范围,并影响低信号样品的分辨能力。因此,建议在实验准备过程中尽量避免强光照射微孔板,或在检测前将微孔板置于暗环境中静置约15分钟,使其磷光信号充分衰减后再进行测量,以降低背景干扰。
滤光片主要用于生物发光共振能量转移(BRET)检测。由于发光信号通常较弱,在滤光片选择上应优先考虑带宽为 80-100 nm的宽频滤光片,以增加有效光信号通过率,从而提高检测灵敏度与信噪比。
报告基因实验将 “调控序列” 与 “报告基因” 结合,用于研究基因表达水平或调控元件活性变化。在实验中,报告基因的遗传信息被导入细胞后,若调控序列被激活,则会驱动报告基因的转录与翻译,产生相应的酶。在底物存在的情况下,酶会催化底物转化并产生光信号。通过检测发光强度,即可间接反映目标调控序列的活性变化。
双荧光素酶报告基因实验(Dual-Luciferase Reporter™ assay, DLR™)在系统中加入了第二种报告基因。除与“调控序列”偶联的报告基因外,还引入了由“管家启动子(housekeeping promoter)”调控的第二种荧光素酶作为内参对照。结合CLARIOstar或VANTAstar酶标仪及其发光扫描功能(luminescence scanning option),可对不同荧光素酶信号进行分辨与优化检测,从而支持多重报告基因体系分析,在单一实验体系中实现多达6种荧光素酶的区分检测。
细胞活性检测中最常见的方法之一是基于萤火虫荧光素酶的ATP依赖型发光,其发光信号强度与细胞内ATP水平正相关:活细胞产生ATP,而细胞裂解释放的ATP作为能量来源驱动荧光素酶催化反应,从而产生发光信号。因此,信号强度可反映细胞数量及整体活性水平。。
除基于 ATP 的终点法细胞活性实验外,发光实验也可实时监测细胞活性。向细胞培养体系中加入“前体底物(pro-substrate)”和萤火虫荧光素酶,前体底物可被活细胞内酶系还原后参与发光反应,从而实现对细胞活性变化的动态追踪。 关于这类实验的更多信息,可参考《实时细胞健康实验:以更少操作获得更优数据》("Real-time cell health assays deliver better data with less effort")。
在药物研发中,该类方法还被广泛用于研究“蛋白水解靶向嵌合体(PROTACs)”和“分子胶(molecular glues)”介导的靶向蛋白降解过程,包括基于 “降解子(degrons)与连接酶(ligases)特异性相互作用” 的靶向蛋白降解研究。

细胞代谢涉及一系列复杂的分子转化过程,目前已有多种基于发光技术的检测方法用于解析不同代谢通路。基础代谢研究通常聚焦于葡萄糖等关键营养物质的利用情况。例如,可通过glucose glo assay直接监测葡萄糖消耗水平;也可通过检测其代谢下游产物乳酸,采用Lactate-Glo™ assay间接反映葡萄糖代谢通量。这两种实验可参考应用说明《基于细胞的实验中,葡萄糖实验与乳酸实验可精准监测细胞葡萄糖代谢》("Glucose assay and lactate assay allow to monitor cellular glucose metabolism precisely in a cell-based assay")。此外,应用说明《基于细胞的 Promega ROS-Glo™实验:发光法检测活性氧》("ROS detection in a cell-based format using the Promega ROS-Glo™ assay")展示了如何利用发光体系检测细胞中过量产生的活性氧(ROS),用于氧化应激水平评估。
受体是重要的药物靶点,其内源性或外源性配体常被用于潜在药物筛选。基于生物发光共振能量转移(BRET)原理,可在细胞水平上研究配体与受体之间的结合行为。实验过程中,可将荧光素酶融合表达于受体的胞外或特定结构域作为供体,而配体则标记相应的荧光团作为受体。当配体与受体结合时,供体与受体之间的空间距离满足能量转移条件,从而发生BRET信号变化,表现为BRET比值升高。
该方法同样适用于未标记化合物的竞争结合研究。未标记化合物可与已知荧光标记配体竞争结合受体,当未标记化合物成功取代标记配体时,BRET信号下降,从而反映结合抑制或位点占据情况(图9)。
关于这类实验在药理学研究的应用,可参考我们的参考文章《受体药理学的实时分析》("Real-time profiling of receptor pharmacology")。

生物发光共振能量转移(BRET)同样可用于解析蛋白质-蛋白质相互作用。在该体系中,将其中一种相互作用蛋白与荧光素酶融合表达作为供体,另一种蛋白与荧光团标记作为受体。当两种蛋白发生相互作用并在空间上接近时,可满足能量转移条件,从而产生BRET信号变化,通常表现为BRET比值升高。该方法可用于研究G蛋白解离(G-protein dissociation)及β-arrestin募集(β-arrestin recruitment)等细胞信号转导过程。
此外,还可采用基于发光的其他方法研究蛋白质相互作用。例如在 《基于内源性 HiBiT CETSA 实验系统检测蛋白质 - 配体结合》("Measuring protein ligand binding with an endogenous HiBiT CETSA test system")中提到的“HiBiT CETSA 法”。该方法通过将片段化的HiBiT纳米荧光素酶与目标蛋白(POI)融合,可用于筛选“蛋白水解靶向嵌合体(PROTACs)”和“分子胶(molecular glues)”介导的靶向蛋白降解,也适用于研究“已知降解子(degrons)与连接酶(ligases)特异性相互作用”引发的靶向蛋白降解。在生理条件下,片段化荧光素酶在生理条件下可重新组装为具有催化活性的完整酶并产生发光信号;而在加热条件下,目标蛋白发生变性会阻碍荧光素酶的组装,从而降低信号输出。若小分子配体与目标蛋白结合,则可提高其热稳定性,使熔点发生可检测的偏移。
除蛋白质 - 蛋白质相互作用检测外,BRET技术还可扩展至各类生物传感器构建,用于特定生物分子的动态检测。例如,研究人员利用CAMYEL BRET生物传感器,分析了合成大麻素受体激动剂对G蛋白信号通路的差异激活作用。
基于微孔板的发光检测通常较其他检测原理具有更高灵敏度。例如,发光酶联免疫吸附实验(ELISA)比比色法实验更灵敏,发光细胞活性检测也优于吸光度法。此外,发光技术适用于多种生物学问题研究,尤其在小体积样品及高通量检测场景中表现突出,其核心优势在于高灵敏度与宽动态范围。然而,发光检测需配备与该技术灵敏度匹配的仪器。
对于非高通量应用,发光检测技术的优势在于“均相实验(homogenous assays)”的可用性。这类实验基于“加样 - 检测(add-and-measure)” 原理,操作简便、快速。同时,多种实时发光体系可用于动态监测细胞过程,实现对生物事件发生过程的定量解析。
功能强大,高度灵敏的HTS酶标仪
用于研发检测的高灵活度酶标仪
灵活简化工作流程的酶标仪
可升级的单模和多模微孔板读数仪系列