
PHERAstar FSX
功能强大,高度灵敏的HTS酶标仪


时间分辨荧光(TRF)技术,可通过引入延迟检测窗口,有效区分背景自发荧光,显著降低背景干扰,提升检测灵敏度与信噪比。 该技术广泛应用于高精度免疫分析及生物分子相互作用研究等领域。
荧光是分子吸收短波长光后,由激发态返回基态过程中释放长波长光的辐射现象。
荧光检测通常分为两类:稳态荧光(steady-state fluorescence)与时间分辨荧光(time-resolved fluorescence, TRF)。两者的核心区别在于所采用荧光团的光物理特性及其发射寿命差异,从而决定了信号采集的时间维度不同。
稳态荧光是最常见的检测模式,通常以“荧光强度”作为读出信号。典型有机荧光团(如荧光素、罗丹明等)的发射寿命处于纳秒量级,激发与发射过程几乎同步发生,因此通常在连续激发条件下实时采集信号。
相比之下,时间分辨荧光(TRF)基于荧光信号的时间衰减行为进行检测。该方法通常采用脉冲激发,并在设定的延迟时间窗口内采集发射信号,因此要求所使用的荧光团具有显著延长的发射寿命(通常为微秒至毫秒级),以区别于背景荧光的快速纳秒衰减。通过在激发后延迟检测,可有效避开短寿命背景信号,从而显著提高检测的灵敏度与信噪比(见图1)。
镧系元素(lanthanides, Ln)是一类具有独特荧光特性的金属元素,通常归属于“稀土元素”范畴。 在发光检测领域,其最显著特征在于极低的本征吸收系数与缓慢的辐射跃迁速率,从而赋予其长发射寿命,通常可达0.5–3 ms量级。镧系元素通常以三价阳离子(Ln³⁺)形式存在,并可在适当配体环境中于水溶液中产生稳定发光信号。此外,其发射光谱呈现窄带特征峰,并具有较大的斯托克斯位移,这使其在复杂生物背景中具备优异的光谱分辨能力与低背景干扰优势 [1]。
镧系元素具备作为生化探针的优良特性。早期研究中,其发光性质被用于模拟和指示Ca²⁺结合行为,作为蛋白质中钙离子结合位点的高灵敏标记工具,为其在生物检测中的应用奠定了基础 [2] 。
基于其长寿命发射特性,镧系荧光团成为时间分辨荧光(TRF)检测体系的理想选择。在实际生命科学应用中,铕(Eu³⁺)、铽(Tb³⁺)、钐(Sm³⁺)和镝(Dy³⁺)是最常用的几类,其中尤以Eu³⁺与Tb³⁺体系应用最为广泛,已成为时间分辨荧光免疫分析等高灵敏检测技术的核心标记体系(见图2)。
铕离子(Eu³⁺)是时间分辨荧光免疫分析中最常用的标记物之一。其不仅具有毫秒级的长发射寿命,还表现出约290 nm的大斯托克斯位移,使激发光谱与发射光谱几乎完全分离,从而显著降低光学串扰与背景干扰。 此外,Eu³⁺在615 nm处具有带宽约10 nm的窄发射峰,谱线高度尖锐,有利于实现高选择性的信号采集与优异的信噪比表现。 (见图3)。[3]
由于镧系离子本身的吸收系数较低,其直接激发所产生的荧光信号通常较弱,难以满足时间分辨荧光(TRF)检测的灵敏度要求。因此,在实际应用中,通常将镧系元素引入具有能量转移功能的配位结构中,以提高其发光效率。这类结构主要包括螯合物(chelates)与穴状化合物(cryptands)。它们可高效吸收外界激发能量,并将能量转移至中心镧系离子,从而显著增强其特征发射信号(见图4)。值得一提的是,此类复合物的激发光谱主要由配体(即“笼状结构”)决定,而非镧系离子本身的吸收特性。[4]
除信号放大作用外,螯合结构还提供了化学修饰位点,使镧系离子能够稳定偶联至抗体、受体或配体等多种生物分子。这一特性是构建时间分辨荧光免疫分析体系的关键基础。
时间分辨荧光(TRF)的检测系统在硬件构成上与常规荧光强度检测类似,主要包括光源系统、波长选择光学组件以及光电倍增管(PMT)检测器。
在光源配置方面,由于镧系元素-配体复合物的典型激发波长集中在约337 nm,TRF检测通常采用氙气闪光灯或脉冲激光作为激发光源。 多功能酶标仪普遍配备宽带氙灯,可兼容荧光、吸光度及发光等多种检测模式;而高端系统则可选配专用TRF激发激光器,在特定波长范围内提供更高能量密度,从而提升低信号检测能力及检测灵敏度。但由于激光器波长固定,其适用范围相对有限,通常专用于TRF及相关高灵敏检测应用。
在波长选择方面,激发光与发射光的分离可通过滤光片系统或光栅单色器实现。相较而言,滤光片系统具有更高的光透过率,因此在光子产率较低的时间分辨荧光检测中通常表现出更高灵敏度。而光栅单色器虽然具备更高的波长可调性,但在TRF及TR-FRET等低信号应用中,由于光通量损失较大,其灵敏度通常受到一定限制。
在时间分辨荧光(TRF)检测中,通常采用光电倍增管(PMT)作为高灵敏度检测器。基于镧系荧光团的长寿命发射特性,PMT在激发脉冲结束后延迟开启检测窗口,使短寿命的自发荧光信号在检测开始前充分衰减,从而实现有效的时间分辨与背景抑制。随后,系统在预设的时间窗口内对发射信号进行积分采集,该过程以时间函数形式对荧光强度进行积分。该检测策略涉及两个关键参数:“积分起始时间”(delay time)与“积分时间”(integration time),通常设定在微秒量级(见图5)。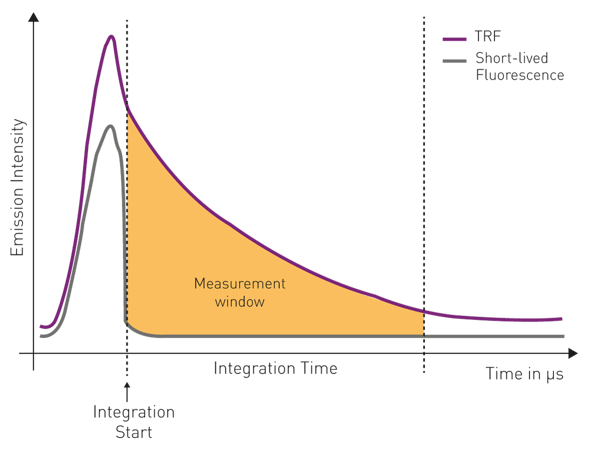
高端酶标仪还可配备用于时间分辨荧光检测的所谓光子计数光电倍增管(PMTs)。与传统积分检测方式不同,常规酶标仪通常仅在设定积分时间内输出荧光信号的累积强度(即时间窗口内的总光子计数或曲线积分值),而光子计数模式则能够以时间分辨方式逐点记录单个光子事件,从而重建镧系荧光团完整的发射衰减曲线。
在 PHERAstar FSX 酶标仪上,光子计数检测可实现约2 μs时间分辨率的数据采集,并输出高精度的荧光衰减曲线。这一功能被称为“衰变曲线监测”(Decay Curve Monitoring),可直观表征荧光寿命特征, 简化TRF方法的开发,并有助于精确优化积分起始时间与积分窗口,从而提升信号分辨能力并有效降低背景干扰。
时间分辨荧光(TRF)免疫检测广泛应用于蛋白质、细胞因子及其他生物标志物的高灵敏定量分析。该方法基于荧光团标记的特异性抗体对靶标分子的高亲和力识别与结合,通过检测时间分辨荧光信号,实现对目标分子的间接定量分析。该技术具有较高的灵敏度与定量能力,并具备多重检测能力,适用于复杂生物体系的分析需求。
在实验流程上, 与酶联免疫吸附试验(ELISA)类似,TRF检测通常在微孔板孔底预包被捕获抗体。加入样品后,目标分子被特异性捕获并固定于固相表面。随后通过洗涤步骤去除未结合成分,再加入与镧系螯合物(常以Eu³⁺为代表)共价偶联的检测抗体,该抗体进一步与靶标分子结合,形成典型的“夹心结构”复合物。再次洗涤后,体系中保留的镧系标记抗体量与靶标分子浓度呈正相关,从而实现定量分析。TRF免疫检测既可采用直接检测模式,也可采用竞争检测模式,以适应不同类型抗原及结合体系的分析需求。
时间分辨荧光免疫检测中通常需要通过“解离-增强”步骤将铕离子从抗体偶联的原始“笼状结构”中释放并重新配位,其原因有以下三点:第一,镧系离子本身光吸收截面较低;第二,其直接激发效率有限;第三,当镧系螯合物与生物大分子(如抗体)偶联后,其发光效率通常进一步下降。
解离过程通过加入一种常称为 “增强液” 的特定溶液来实现。该试剂不仅能够促使镧系离子从原有螯合配位环境中解离,还会诱导其在溶液中重新形成具有高发光效率的二次螯合结构。新的配位结构可有效吸收激发光能,并通过分子内能量转移将能量传递至镧系离子,从而显著增强其特征发射信号强度(图6)。
样品由特定波长(通常为 337 nm)的光脉冲激发。整个检测采用时间门控策略:在激发结束后,系统首先设置延迟时间,使纳秒至微秒量级的短寿命自发荧光充分衰减;随后开启检测窗口,仅采集长寿命镧系荧光信号,从而实现对目标信号的选择性提取。在信号采集阶段,发射光于预设时间窗口内进行积分,并以积分强度作为最终读出值,而非记录完整的衰减曲线。由于该积分信号与分析物浓度呈线性相关,因此可通过标准曲线实现定量分析
DELFIA® 是目前应用最广泛的时间分辨荧光免疫分析方法之一。
DELFIA(解离增强镧系荧光免疫检测法,Dissociation-Enhanced Lanthanide Fluorescent Immunoassay)是一种典型的异相时间分辨荧光检测体系,包含标准洗涤步骤,其基本原理与酶联免疫吸附试验(ELISA)类似。相较于ELISA,DELFIA通常具有更宽的动态范围与更高的信噪比,并且在反应结束后信号可长期保持稳定(可达数月),便于重复读取与数据验证。在仪器要求方面,DELFIA检测需要配备时间分辨荧光检测功能,典型参数为激发波长约337 nm、发射波长约615 nm(Eu³⁺特征发射)。
在 DELFIA 检测中,捕获抗体首先固定于微孔板表面;加入样品孵育后,靶标分子被特异性捕获并富集于固相表面。经洗涤去除未结合组分后,引入铕标记的检测抗体形成免疫复合物。完成最终洗涤后加入增强液,使镧系离子从原始螯合环境中解离,并在溶液中重新形成高效发光的配位复合物,从而产生强时间分辨荧光信号。相关实验流程可参考《使用匹配抗体对试剂盒和 PHERAstar FSX 酶标仪在384 孔板进行时间分辨荧光(TRF)免疫检测》。
尽管 DELFIA 检测具有优异的灵敏度与方法学稳健性,但由于其依赖多步孵育与洗涤流程,整体操作时间较长,因此在超高通量筛选应用中存在一定限制。
外泌体是来源于内体途径形成的细胞外囊泡,富含核酸、蛋白质及脂质等多种生物分子,在细胞间信号传递与信息交流中发挥重要作用。因此,外泌体已成为疾病生物标志物研究及液体活检领域的重要分析对象。TRIFic™时间分辨荧光外泌体检测试剂盒可基于外泌体表面特征膜蛋白的表达情况,实现对外泌体的特异性检测与定量分析,从而用于外泌体水平及相关生物学过程的研究。
目前已有多种对氧气及pH变化敏感的荧光探针,可在时间分辨荧光(TRF)模式下用用于细胞代谢参数的定量分析。在相关应用研究中,该技术能够在活细胞体系中实时监测氧气消耗及糖酵解过程,从而实现对细胞能量代谢状态的连续性评估与动态解析。
时间分辨荧光的另一项重要应用方向为 TR-FRET(时间分辨荧光共振能量转移)技术。该技术结合了时间分辨检测与能量转移机制,具有信号稳定性高、背景干扰低、易于自动化及适配微孔板高通量筛选等优势,因此被广泛应用于药物筛选及大规模生物分子相互作用分析。其主要应用场景包括蛋白质-蛋白质相互作用研究以及配体-受体结合过程的检测与筛选分析。
所有生物样品中均不可避免地存在一定程度的自发荧光,这通常是限制检测灵敏度的关键因素。由于自发荧光及激发光散射的寿命通常处于纳秒级别,因此在时间分辨荧光(TRF)检测中,可通过设置微秒至毫秒级的时间门控,在短寿命背景信号完全衰减后再采集镧系元素的长寿命发射信号,从而实现有效的时间选择性检测。通过该检测,短寿命背景信号被显著滤除,最终检测背景主要来自非特异性结合的标记物,相较于稳态荧光检测,TRF可明显降低背景干扰并提升整体检测灵敏度。
斯托克斯位移定义为激发光最大吸收波长与发射光最大波长之间的差值。对于多数传统稳态荧光团而言,其斯托克斯位移相对较窄,且激发与发射光谱存在一定重叠,容易引发自吸收或信号猝灭,从而降低检测效率。 相比之下,镧系元素具有显著更大的斯托克斯位移,使激发与发射光谱实现良好分离,从而有效减少光谱串扰并显著提高时间分辨荧光检测中的信噪比(S/B)。
镧系元素通常具有较高的量子产率,其发射信号强度优于多数传统荧光标记物,从而显著提升检测灵敏度。需要注意的是,由于其光物理特性,高量子产率使镧系离子更适合作为能量转移体系中的供体,而不适合作为受体使用。
据厂商数据,在时间分辨荧光免疫检测中,若在解离/增强步骤前终止反应并妥善保存,检测体系可保持极高稳定性,最长可达10年。后续仅需加入增强液即可重新激活发光信号,实现重复检测与数据再读取,从而提高实验数据的利用效率。
镧系元素通常以螯合物或穴状配位结构形式存在,以实现信号放大及与生物分子的稳定偶联。在实际检测过程中,还需通过“解离-增强”步骤,使镧系离子从原有配位环境中释放并重新形成高发光效率的复合物,从而获得可检测的强荧光信号。在原始状态下,镧系离子的发射强度通常较低,因此该步骤对信号输出至关重要。这一过程通常依赖多次洗涤、孵育及试剂添加等操作步骤,显著增加了实验流程的复杂性与操作时间。相比之下,传统基于荧光强度的检测方法多可直接读取信号,无需额外后处理步骤,在操作更为简便。
尽管时间分辨荧光(TRF)在灵敏度与信噪比方面具有显著优势,但其对专用试剂(如镧系元素)及检测设备(具备时间门控能力的酶标仪)的依赖,使整体实验成本高于常规荧光强度检测方法。
时间分辨荧光检测采用顶部读取模式,优先选用白色微孔板。白色孔壁具有高反射率,可有效增强发射信号;结合时间门控策略对背景信号的抑制,可进一步提升整体检测灵敏度。当信号强度过高、存在检测器饱和风险时,可改用黑色微孔板以降低反射信号,从而优化检测动态范围。
在部分应用中,也可选择具有白色或黑色孔壁且底部透明的微孔板,并结合底部读取模式进行检测。然而需要注意,并非所有透明孔底材料均具备良好的紫外透光性能。某些塑料材料在约340 nm波段(典型TRF激发波长为337 nm)存在显著吸收,可能降低激发效率并影响检测灵敏度。
因此,在实验设计阶段,应优先选择具备紫外透过特性的微孔板材料,并确认其光学参数符合TRF检测需求,以确保实验结果的稳定性与可靠性。更多细节可参考《微孔板:实际应用中的实用性》。
时间分辨荧光检测虽能够有效消除自发荧光背景,但在镧系标记试剂孵育后、加入增强液之前的洗涤步骤仍然是决定检测质量的关键环节。该步骤必须充分且高效,以彻底去除所有未结合或非特异性结合的标记物。若洗涤不充分,残留的游离镧系离子或标记抗体将显著提高背景信号,从而降低检测信噪比与定量准确性。
在 DELFIA 检测中,应优先选用基于 TRIS-HCl 的缓冲液,而非磷酸盐缓冲液。一方面,高浓度磷酸盐在长时间孵育条件下可能影响铕离子稳定性,导致其从螯合结构中部分解离;另一方面,与TRIS-HCl体系相比,磷酸盐缓冲液通常会降低最终信号强度,影响检测灵敏度。
低pH环境可能破坏镧系螯合物的稳定性,导致金属离子释放,从而增加非特异性背景信号并降低检测可靠性。此外,应特别注意试剂体系中是否含有EDTA等金属螯合剂,因为EDTA会与镧系离子发生竞争性络合,导致标记体系失活。
镧系元素的发射光不具有偏振特性 因此它们无法用于各向异性 / 荧光偏振测量类检测方法。[5]
DELFIA 为珀金埃尔默公司的注册商标。
功能强大,高度灵敏的HTS酶标仪
用于研发检测的高灵活度酶标仪
灵活简化工作流程的酶标仪
可升级的单模和多模微孔板读数仪系列